|
On sait que les maladies héréditaires peuvent être hétérogènes. En effet, l'ÔŅĹge de début, les signes cliniques, les atteintes d'autres organes, l'ÔŅĹge de survenue de l'insuffisance rénale, etc., peuvent varier d'un sujet à l'autre.
Parfois, il existe des différences d'une famille à l'autre, mais à l'intérieur d'une même famille, la ressemblance est grande entre les sujets atteints.
Parfois, les différences existent non seulement entre familles, mais également entre sujets de la même famille.
Chaque gène dirige la fabrication d'une protéine. Les protéines peuvent être considérées comme les machines-outils qui font fonctionner tout l'organisme.
Chaque protéine est composée par des acides aminés qui se succèdent en ordre précis; cet ordre assure le bon fonctionnement de la protéine
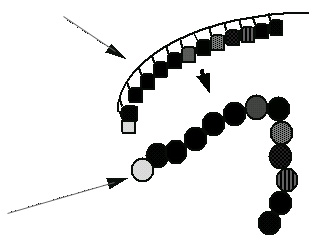
La succession normale des acides aminés dépend de la succession des bases sur le gène. Voici un gène normal sur lequel des bases se succèdent
| |
 |
|
| |
Voici la protéine normale correspondant à ce gène ;
elle est faite d'acides aminés correspondant aux bases. |
|
Une mutation est une modification d'un gène. Et par conséquent, la protéine, qui est le produit du gène, peut être absente ou défectueuse. On dit que le gène modifié est un gène muté.
*Il existe une grande variété de mutations dépendant de leur localisation dans le gène et de leur type.
La mutation peut siéger à des endroits différents dans le gène, et certains endroits sont plus importants que d'autres pour le bon fonctionnement du gène;
*la mutation peut aller d'un changement d'une base à une disparition d'une plus ou moins grande partie du gène. En voici deux exemples sur le schéma:
*plusieurs bases manquent (c'est une délétion) ;
*une base est changée en une autre (c'est une mutation ponctuelle).
| |
 |
|
| |
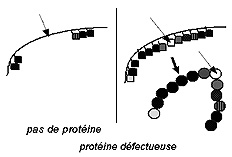
Sur le schéma de gauche, il manque plusieurs bases;
la protéine ne peut être fabriquée.
Sur le schéma de droite, une base est modifiée (base noire remplacée par une base blanche); la protéine est fabriquée, mais fonctionne mal. |
|
Toute maladie héréditaire est provoquéepar une mutation d'un gène.Tous les membres d'une même famille, s'ils sont atteints, ont la même mutation dans le même gène. Mais d'une famille à l'autre, les mutations peuvent être différentes.
En partant de ce qui se passe dans le gène, on peut distinguer plusieurs situations. Mais, nous verrons que, pour une même maladie, ces différentes situations peuvent s'imbriquer.
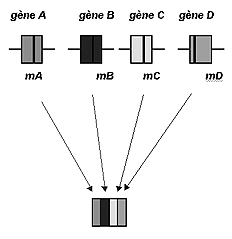
LPlusieurs gènes sont impliqués dans la survenue de la maladie. La maladie X peut être provoquée par une mutation du gène A dans une famille, une mutation du gène B dans une autre famille, etc.
Ces gènes (figurés par les rectangles sur la figure ci-dessous) peuvent être situés sur le même chromosome ou sur des chromosomes différents. La mutation m est figurée par le trait vertical.
Bien des gènes ayant été trouvés, la Génétique permet maintenant d'éviter aux patients des explorations invasives.
Prenons l'exemple de la NEPHRONOPHTISE, dont le gène a été trouvé dans le groupe de Marie-Claire Gubler par Corinne Antignac. Jadis, il fallait une biopsie rénale et une étude anatomo-pathologique du fragment de rein prélevé pour arriver au diagnostic. Maintenant, une prise de sang de 5 millilitres chez un enfant, dont l'histoire clinique est évocatrice de NEPHRONOPHTISE, permet d'extraire le DNA des globules blancs pour rechercher l'anomalie moléculaire caractéristique (présente chez environ 90 % des patients).
Voici un autre exemple, celui de l'AMYOTROPHIE SPINALE (qui entraîne une paralysie des quatre membres à la naissance). Jusqu'à une date récente, il fallait de nombreux examens souvent pénibles, et en particulier, une biopsie du muscle et des électromyogrammes. Une prise de sang maintenant permet d'arriver au diagnostic de la maladie (dans 90 % des cas).
| |
 |
|
| |
Les différentes formes de la Maladie X. |
|
On conçoit que la maladie X puisse être différente entre la famille A (le gène A est muté) et la famille B (le gène B qui est muté), etc.,
Citons comme exemple la Polykystose rénale dominante autosomique. Les néphrologues avaient remarqué que l'évolution vers l'insuffisance rénale terminale était plus tardive dans certaines familles. Les deux gènes dont les mutations sont responsables de l'apparition de la maladie sont maintenant connus:
*le gène PKD1 (situé sur le chromosome 16);
*le gène PKD2 (situé sur le chromosome 2).
On a montré que l'évolution vers l'insuffisance rénale était plus tardive dans la forme liée au gène PKD2 que dans la forme liée au gène PKD1.
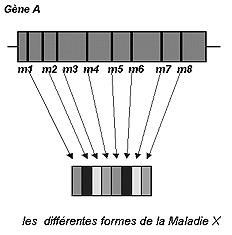
Considérons un gène, le gène A, impliqué dans la survenue de la maladie. Les mutations sont le plus souvent différentes d'une famille à l'autre: dans une famille c'est la mutation m1, dans une autre la mutation m2, etc.
Pour certaines maladies, les mutations sont très nombreuses et on considère que "chaque famille a sa mutation". Pour d'autres maladies, une mutation est plus fréquente que les autres et se retrouve dans un grand nombre de familles. On retrouve, par exemple, la mutation m1 dans 85% des familles et les autres mutations (m2, m3, m4,...) se répartissent entre les autres familles. Parfois, les mutations sont différentes d'un pays à l'autre (la mutation m1 très fréquente en France et la mutation m2 très fréquente en Italie).
| |
 |
|
| |
Les différentes formes de la Maladie X. |
|
On conçoit que l'atteinte clinique dans les familles ayant la mutation m1 puisse être différente de l'atteinte clinique dans les familles ayant la mutation m2, elle-même différente de l'atteinte clinique des familles ayant la mutation m3, etc.
Actuellement, des groupes d'études réunissant cliniciens et généticiens tentent de montrer des correspondances entre les caractéristiques cliniques de la maladie (rénale ou non rénale) et la mutation
elle-même. En langage de généticien, les caractéristiques cliniques s'appellent phénotype et les caractéristiques du DNA s'appellent génotype.
On peut citer comme exemple la maladie de von Hippel-Lindau. Cette maladie est caractérisée par une prédisposition au développement de tumeurs dans le cerveau, la rétine, les reins et les glandes surrénales. Le gène est localisé sur le chromosome 3. De nombreuses mutations sont connues. Les cliniciens avaient remarqué que, dans certaines familles, les sujets atteints présentaient une tumeur de la surrénale et que, dans d'autres familles, aucun sujet atteint ne présentait de telle tumeur. Les études en génétique moléculaire ont mis en évidence une mutation particulière dans les premières familles. Ce fait a une conséquence pratique d'importance. Lorsqu'on trouve cette mutation particulière dans une famille atteinte de maladie de von Hippel-Lindau, la surveillance radiologique et clinique des glandes surrénales est renforcée afin de dépister une tumeur le plus précocement possible.
Prenons un autre exemple, celui du syndrome d'Alport. L' European Community Alport Syndrome Concerted Action (dirigée par le Dr Marie-Claire Gubler) a réuni néphrologues, anatomopathologistes et généticiens de 12 groupes appartenant à 12 pays européens. Des informations sur les patients de 330 familles atteintes de syndrome d'Alport ont été recueillies. Un des buts de ce travail est de rechercher les relations entre le type et la localisation de la mutations et la clinique et de reconnaître, en particulier, les mutations responsables d'une insuffisance rénale précoce ou d'une surdité.
Dans la cystinose, on sait que les premiers symptômes, la maladie rénale, la sévérité de l'évolution sont homogènes d'un enfant à l'autre; ils ne paraissent pas dépendre de la mutation en cause. Mais les atteintes extra-rénales de la cystinose différent d'un enfant à l'autre. Une étude en cours permettra de savoir si les manifestations extra-rénales ne sont pas, elles, liées au type de mutation.
L'exemple le plus illustratif est celui du SYNDROME D'ALPORT. Cette maladie rénale résulte tantôt d'une mutation d'un gène sur le chromosome X, tantôt d'une mutation d'un gène situé sur le chromosome 2. En présence d'une femme enceinte qui nous dit qu'elle-même est atteinte ou que son mari est atteint, il est essentiel de déterminer le mode d'hérédité afin d'apprécier le risque pour ses descendants.
Si le syndrome est lié à un gène sur le chromosome X, il y a un risque pour les enfants : la femme atteinte peut transmettre le chromosome X porteur du gène déficient à ses garçons ou à ses filles ; l'homme atteint transmet le chromosome X à ses filles, qui peuvent le transmettre à leur tour.
La situation est différente s'il s'agit d'une hérédité récessive : chaque personne contribue par moitié à la transmission et il n'y a aucun risque pour les descendants. Dans cette situation, le généticien rassure totalement.
Lorsque la famille est grande et que plusieurs individus sont déjà atteints, le généticien peut, au vu de l'arbre généalogique, déterminer le mode de transmission et répondre à cette femme. Mais que peut-il lui répondre si la famille est petite, si un seul individu est atteint ? Cette situation est dramatique. Des techniques mises au point sur biopsie de peau par Marie-Claire Gubler permettent parfois de répondre. Mais dans un certain nombre de cas, il est indispensable faire une étude génétique de la famille afin de rechercher les mutations.
Cependant, comme nous le verrons plus loin, les moyens financiers manquent actuellement pour mener à bien ces tests génétiques.
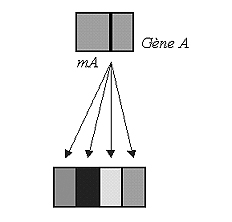
Un seul gène, le gène A, est impliqué. On trouve la même mutation, mA, dans toutes les familles. Les sujets d'une même famille présentent cependant des formes différentes de la maladie X.
| |
 |
|
| |
Les différentes formes de la maladie X |
|
Reprenons l'exemple de la Polykystose rénale dominante autosomique.
1. Dans une famille, un sujet développe une insuffisance rénale terminale précocement alors que son frère ne présente pas d'insuffisance rénale avant un ÔŅĹge avancé.
2. Dans une famille, un nouveau-né présente des reins volumineux à la naissance. Cette forme néonatale peut amener à découvrir que l'un de ses parents (le père ou la mère) a des reins kystiques et de taille augmentée. La Polykystose rénale, découverte tardivement chez ce parent adulte, était jusque là passée inaperçue.
Comment l'expliquer ces différences ? Dans la première famille, il est logique de penser en premier lieu à des facteurs d'environnement chez les 2 frères. La consommation de tabac, le régime alimentaire, le mode de vie, le contrôle de l'hypertension artérielle, etc., ne sont ils pas différents chez les 2 frères ? Ces facteurs d'environnement ne pourraient-ils pas influencer l'apparition plus ou moins précoce de l'insuffisance rénale ? Mais on sait aussi que, si ces 2 frères ont tous deux hérité de la même mutation du gène PKD, leurs autres gènes ne sont pas identiques. L'un de ces autres gènes ne pourrait-il pas modifier l'allure générale de la maladie ?
Dans la seconde famille, le nouveau-né a hérité la mutation du gène PKD de l'un de ses parents. Mais ses autres gènes ne sont pas identiques à ceux de ce parent. L'un de ces gènes n'est-il pas responsable de la gravité de la maladie ?
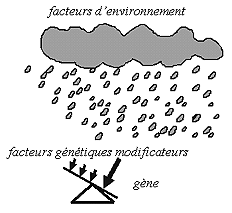
On appelle gènes modificateurs des gènes pouvant moduler l'expression ou l'évolution d'une maladie. Depuis longtemps, les généticiens ont évoqué cette possibilité pour expliquer les variations cliniques d'une même maladie. Mais ce n'est que depuis peu que cette hypothèse trouve un appui dans quelques exemples chez l'animal et dans quelques maladies génétiques humaines. On peut conclure actuellement que les mécanismes d'action de ces gènes modificateurs sont variés. Leur découverte pourra peut-être à l'origine de nouveaux traitements.
| |
 |
|
| |
Les différents facteurs |
|
La variabilité d'une maladie est un phénomène complexe à étudier. Les chercheurs travaillant sur les maladies héréditaires, qu'elles soient rénales ou non rénales, se posent de nombreuses questions actuellement.
Reprenons l'exemple de la Polykystose rénale dominante autosomique.
*Deux gènes, PKD1 et PKD2, sont impliqués, ce qui explique en partie les différences d'évolution entre familles.
*Dans le gène PKD1, on trouve de nombreuses mutations. Existe-t-il une correspondance entre d'une part le type et la localisation de la mutation dans le gène et d'autre part l'association à des atteintes d'autres organes (anévrisme des artères cérébrales) dans certaines familles ou bien une évolution plus ou moins rapide vers l'insuffisance rénale terminale ?
*La maladie peut être différente entre sujets atteints de la même famille qui ont la même mutation? Ces différences sont-elles dues à des facteurs d'environnement ou à des gènes modificateurs ou aux deux ?
Textes rédigées par le Dr Micheline Levy. Unité 535 INSERM, Paris.
|
|